- 首页 > 正文
什么是CKD相关心肌病?
发表时间:2025-05-23 16:23:51
编者按:慢性肾脏病(CKD)相关心肌病发病率高,病理生理学机制复杂,CKD一系列并发症也与心肌病相互作用,对患者预后产生严重影响,患者的综合管理是临床医生面临的重大挑战。本文结合《慢性肾脏病相关心肌病综合管理中国专家共识(2024版)》[1](以下简称“共识”)对CKD相关心肌病进行介绍,期望有助于临床工作者更好地了解这一疾病,以更好地应对这一挑战。
心肌病是慢性肾脏病(CKD)常见的心血管并发症之一。CKD相关心肌病定义为由于CKD相关因素导致的心肌损伤和/或功能障碍(需排除原发性心肌病、其他心血管疾病和全身系统性疾病,如淀粉样变、Fabry病等),其主要特征为左心室肥厚(LVH)和左心室质量指数(LVMI)增加,伴或不伴左心室舒张和/或收缩功能障碍。CKD相关心肌病在组织学上常存在心肌纤维化。
一、影响CKD相关心肌病患者结局的危险因素
肾功能损害(如肾小球滤过率[GFR]降低)、肾脏结构破坏(如白蛋白尿)以及与肾脏疾病相关的并发症都显著影响CKD相关心肌病患者的结局。这些危险因素与心脏结构和功能的改变密切相关,如LVH、左心室收缩和舒张功能不良,以及心肌纤维化。此外,高血压、糖尿病、肥胖、高血脂等也是影响CKD相关心肌病患者结局的重要因素(图1)[2]。因此,在临床实践中,综合评估这些危险因素对于预测和改善CKD相关心肌病患者的预后具有重要意义。
共识推荐对CKD患者常规筛查心肌病相关的常见危险因素,寻找可改善的危险因素并给予控制(如控制高血压、降低蛋白尿、减轻水钠潴留、控制透析间期容量增长、清除尿毒症毒素、纠正CKD相关并发症等),从而延缓CKD相关心肌病的发生或减轻该病的进展及严重程度。
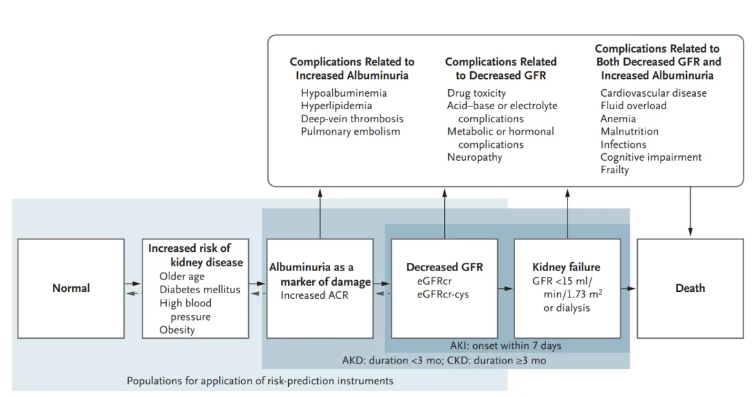
图1. 通过肾小球滤过率(GFR)和白蛋白尿水平来确定急、慢性肾脏病的发生、进展和并发症
二、CKD相关心肌病
01心肌肥厚
CKD相关心肌病的主要和早期表现是LVH,心脏结构重塑,随着肾功能的下降,LVH的风险显著增加。透析患者的CKD心肌病患病率明显增加,终末期肾病(ESRD)患者高达75%至89%。肾功能下降的不同阶段与左心室形状结构异常有关,心脏肥大和心脏结构重塑,可引起心脏电生理功能紊乱,并增加猝死风险(图2)。CKD患者可有不同程度的向心性重构、离心性肥厚、向心性肥厚。虽然这些特征常见于需要肾脏替代治疗(KFRT)的终末期CKD患者,但eGFR轻度至中度降低的患者已经表现出与CKD相关心肌病一致的结构和功能改变。eGFR与左心室几何形状有显著相关性,eGFR越低,患者越容易出现向心性肥厚[3,4]。
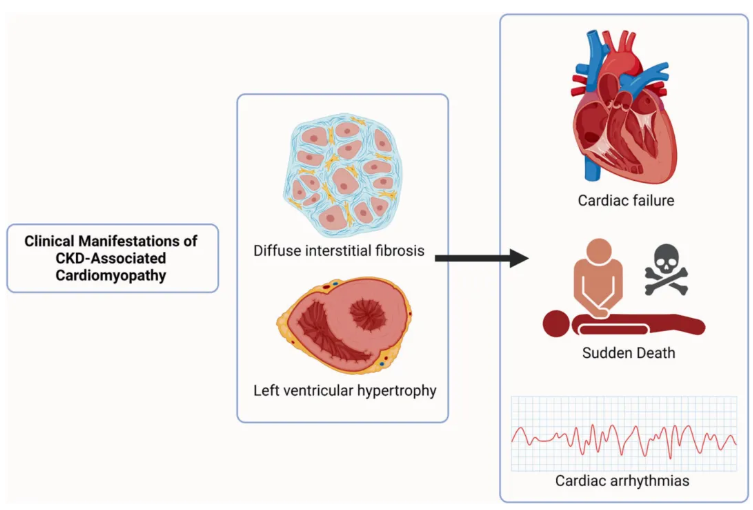
图2. CKD相关心肌病心肌结构和功能改变
02收缩和舒张功能不良
CKD患者的左心室舒张功能障碍非常普遍,KFRT患者中甚至高达85%至90%。LVH与舒张功能障碍有关,CKD患者肾功能下降会导致左心室舒张功能不良。舒张功能障碍还可能是导致透析患者肺水肿、透析中低血压频繁发生的原因。目前认为,未经控制的高血压可能通过增加后负荷、导致心肌病变和增加左心室壁的僵硬度,从而降低左心室顺应性,进而导致左心室舒张功能减低[4]。心肌的收缩功能可以通过整体纵向应变(global longitudinal strain,GLS)反应,GLS指整体心肌纵向应变大小,是所有心肌节段纵向峰值应变的平均值。CKD患者左心室重构常导致收缩功能不全,一项对左心室射血分数≥50%的透析前和透析患者的研究发现,与LV GLS>15.2%的患者相比,LV GLS≤15.2%的患者的CKD更晚期、透析时间更短、心率更高,相关合并症的患病率更高,口服抗凝药物的使用率更高,且白蛋白水平更低[5]。
03心肌纤维化
心肌纤维化是指心肌组织中胶原纤维和其他细胞外基质成分的过量沉积,导致心肌组织的结构和功能发生改变。左室功能受损的透析患者中,心肌活检显示间质纤维化,严重的肌细胞肥大、排列紊乱。心肌纤维化是心源性死亡的预测指标,对于发生严重心肌纤维化的透析患者而言,密切监测和及时治疗非常关键。对比增强心脏磁共振(cardiac magnetic resonance, CMR)成像已被用于评估心肌梗死、扩张型和肥厚型心肌病等情况下的心肌纤维化(图3)。非对比剂心肌固有T1弛豫时间已成为评估CKD/KFRT心肌纤维化的可行替代方法。KFRT患者的初始T1时间增加,并与左心室质量(LVM)增加相关[6,8]。
共识推荐在CKD G3b以后有条件的患者可进行1次心脏磁共振成像 (CMR)检查。
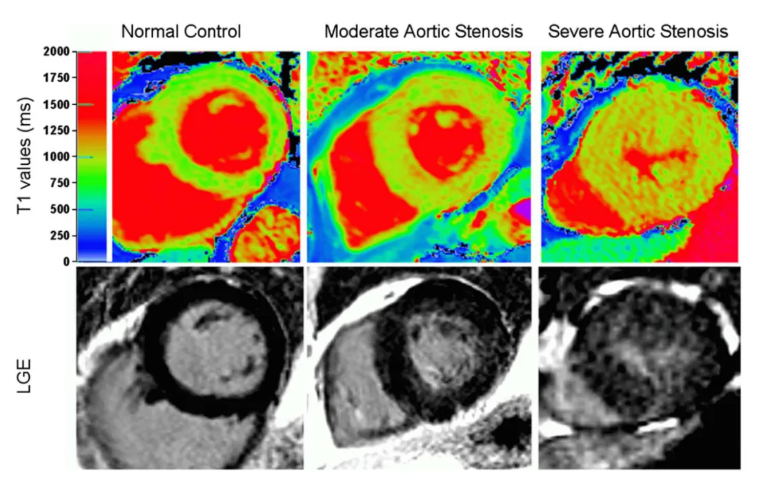
图3. 心脏磁共振成像(CMR) 图像分析
三、CKD相关心肌病的发病机制
01心脏后负荷增加
高血压、主动脉瓣狭窄、动脉硬化等可通过影响血流动力学改变诱发心肌肥厚。此外,血压升高继发的RAAS 激活、尿毒症毒素、慢性肾脏病矿物质和骨代谢异常(CKD-MBD)、晚期糖基化终末产物、炎症、氧化应激等均可导致动脉硬化,血管顺应性降低,加重心肌后负荷,导致LVH、心肌纤维化和舒张功能障碍[9]。
02心脏前负荷增加
CKD患者GFR降低和RAAS激活更容易发生水钠潴留,循环系统的血容量增加,加重了心肌的前负荷[10]。贫血时氧气输送减少,交感神经活动增强,心率加快和心肌收缩力增强,迫使心脏泵出更多的血液,进而增加了前负荷[11]。动脉静脉内瘘(AVF)是一种血管外科手术,将患者的动脉和静脉通过手术连接建立血管通路,这种手术常用于长期血液透析的CKD患者,能够降低感染风险和死亡率,降低维持血管畅通的干预因素。AVF导致局部区域的血液从动脉向静脉循环的高流量分流,使低压力、高容量的静脉系统暴露于高压力、低容量的动脉系统,降低了全身血管的总阻力,同时增加静脉回流到心脏,增加了心排血量[12]。
03CKD患者内环境异常
CKD患者的心肌病变是由多种复杂的内环境紊乱相互作用引起的,包括RAAS激活、交感神经活跃、转化生长因子-β(TGF-β)信号传导增加、胰岛素抵抗、尿毒症毒素(如硫酸吲哚酚、对甲酚等)、强心甾类固醇(包含强心苷类,如地高辛)、氧化应激和与CKD-MBD相关的因素如甲状旁腺功能亢进、维生素D缺乏、FGF-23、Klotho降低和高磷血症等。这些因素共同作用,导致心肌细胞损伤、肥厚和纤维化,最终可能发展为心力衰竭(HF)(图4)[13]。
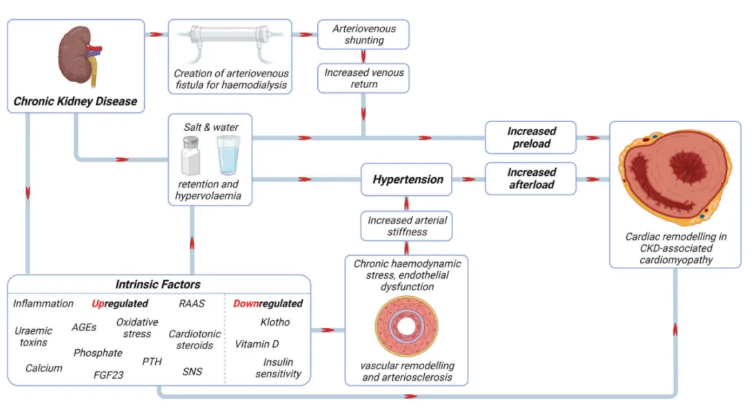
图4. CKD相关心肌病的发病机制
参考文献
[1]中国血液净化. 2024年8月, 第23卷, 第8期: 561-580.
[2]N Engl J Med 2022;386:2120-8.
[3]Journal of Human Hypertension (2023) 37:1–19.
[4]J Am Soc Nephrol. 2012 Sep 28; 23(10): 1725–1734.
[5]European Journal of Heart Failure (2018)20, 560–568.
[6]Nephrol Dial Transplant (1990) 5: 39-44.
[7]Kidney International, Vol. 67 (2005), pp. 333–340.
[8]Heart 2013;99:932–937.
[9]Hemodial Int. 2008;12:322–7.
[10]Journal of the American Society of Nephrology?28(8):p 2491-2497.
[11]Nephrol Dial Transplant (2000) 15 [Suppl 3]: 14–18.
[12]European Heart Journal (2017) 38, 1913-1923.
[13]Nat Rev Nephrol. 2019 Mar;15(3):159-175.
心肌病是慢性肾脏病(CKD)常见的心血管并发症之一。CKD相关心肌病定义为由于CKD相关因素导致的心肌损伤和/或功能障碍(需排除原发性心肌病、其他心血管疾病和全身系统性疾病,如淀粉样变、Fabry病等),其主要特征为左心室肥厚(LVH)和左心室质量指数(LVMI)增加,伴或不伴左心室舒张和/或收缩功能障碍。CKD相关心肌病在组织学上常存在心肌纤维化。
一、影响CKD相关心肌病患者结局的危险因素
肾功能损害(如肾小球滤过率[GFR]降低)、肾脏结构破坏(如白蛋白尿)以及与肾脏疾病相关的并发症都显著影响CKD相关心肌病患者的结局。这些危险因素与心脏结构和功能的改变密切相关,如LVH、左心室收缩和舒张功能不良,以及心肌纤维化。此外,高血压、糖尿病、肥胖、高血脂等也是影响CKD相关心肌病患者结局的重要因素(图1)[2]。因此,在临床实践中,综合评估这些危险因素对于预测和改善CKD相关心肌病患者的预后具有重要意义。
共识推荐对CKD患者常规筛查心肌病相关的常见危险因素,寻找可改善的危险因素并给予控制(如控制高血压、降低蛋白尿、减轻水钠潴留、控制透析间期容量增长、清除尿毒症毒素、纠正CKD相关并发症等),从而延缓CKD相关心肌病的发生或减轻该病的进展及严重程度。

图1. 通过肾小球滤过率(GFR)和白蛋白尿水平来确定急、慢性肾脏病的发生、进展和并发症
二、CKD相关心肌病
01心肌肥厚
CKD相关心肌病的主要和早期表现是LVH,心脏结构重塑,随着肾功能的下降,LVH的风险显著增加。透析患者的CKD心肌病患病率明显增加,终末期肾病(ESRD)患者高达75%至89%。肾功能下降的不同阶段与左心室形状结构异常有关,心脏肥大和心脏结构重塑,可引起心脏电生理功能紊乱,并增加猝死风险(图2)。CKD患者可有不同程度的向心性重构、离心性肥厚、向心性肥厚。虽然这些特征常见于需要肾脏替代治疗(KFRT)的终末期CKD患者,但eGFR轻度至中度降低的患者已经表现出与CKD相关心肌病一致的结构和功能改变。eGFR与左心室几何形状有显著相关性,eGFR越低,患者越容易出现向心性肥厚[3,4]。

图2. CKD相关心肌病心肌结构和功能改变
02收缩和舒张功能不良
CKD患者的左心室舒张功能障碍非常普遍,KFRT患者中甚至高达85%至90%。LVH与舒张功能障碍有关,CKD患者肾功能下降会导致左心室舒张功能不良。舒张功能障碍还可能是导致透析患者肺水肿、透析中低血压频繁发生的原因。目前认为,未经控制的高血压可能通过增加后负荷、导致心肌病变和增加左心室壁的僵硬度,从而降低左心室顺应性,进而导致左心室舒张功能减低[4]。心肌的收缩功能可以通过整体纵向应变(global longitudinal strain,GLS)反应,GLS指整体心肌纵向应变大小,是所有心肌节段纵向峰值应变的平均值。CKD患者左心室重构常导致收缩功能不全,一项对左心室射血分数≥50%的透析前和透析患者的研究发现,与LV GLS>15.2%的患者相比,LV GLS≤15.2%的患者的CKD更晚期、透析时间更短、心率更高,相关合并症的患病率更高,口服抗凝药物的使用率更高,且白蛋白水平更低[5]。
03心肌纤维化
心肌纤维化是指心肌组织中胶原纤维和其他细胞外基质成分的过量沉积,导致心肌组织的结构和功能发生改变。左室功能受损的透析患者中,心肌活检显示间质纤维化,严重的肌细胞肥大、排列紊乱。心肌纤维化是心源性死亡的预测指标,对于发生严重心肌纤维化的透析患者而言,密切监测和及时治疗非常关键。对比增强心脏磁共振(cardiac magnetic resonance, CMR)成像已被用于评估心肌梗死、扩张型和肥厚型心肌病等情况下的心肌纤维化(图3)。非对比剂心肌固有T1弛豫时间已成为评估CKD/KFRT心肌纤维化的可行替代方法。KFRT患者的初始T1时间增加,并与左心室质量(LVM)增加相关[6,8]。
共识推荐在CKD G3b以后有条件的患者可进行1次心脏磁共振成像 (CMR)检查。

图3. 心脏磁共振成像(CMR) 图像分析
三、CKD相关心肌病的发病机制
01心脏后负荷增加
高血压、主动脉瓣狭窄、动脉硬化等可通过影响血流动力学改变诱发心肌肥厚。此外,血压升高继发的RAAS 激活、尿毒症毒素、慢性肾脏病矿物质和骨代谢异常(CKD-MBD)、晚期糖基化终末产物、炎症、氧化应激等均可导致动脉硬化,血管顺应性降低,加重心肌后负荷,导致LVH、心肌纤维化和舒张功能障碍[9]。
02心脏前负荷增加
CKD患者GFR降低和RAAS激活更容易发生水钠潴留,循环系统的血容量增加,加重了心肌的前负荷[10]。贫血时氧气输送减少,交感神经活动增强,心率加快和心肌收缩力增强,迫使心脏泵出更多的血液,进而增加了前负荷[11]。动脉静脉内瘘(AVF)是一种血管外科手术,将患者的动脉和静脉通过手术连接建立血管通路,这种手术常用于长期血液透析的CKD患者,能够降低感染风险和死亡率,降低维持血管畅通的干预因素。AVF导致局部区域的血液从动脉向静脉循环的高流量分流,使低压力、高容量的静脉系统暴露于高压力、低容量的动脉系统,降低了全身血管的总阻力,同时增加静脉回流到心脏,增加了心排血量[12]。
03CKD患者内环境异常
CKD患者的心肌病变是由多种复杂的内环境紊乱相互作用引起的,包括RAAS激活、交感神经活跃、转化生长因子-β(TGF-β)信号传导增加、胰岛素抵抗、尿毒症毒素(如硫酸吲哚酚、对甲酚等)、强心甾类固醇(包含强心苷类,如地高辛)、氧化应激和与CKD-MBD相关的因素如甲状旁腺功能亢进、维生素D缺乏、FGF-23、Klotho降低和高磷血症等。这些因素共同作用,导致心肌细胞损伤、肥厚和纤维化,最终可能发展为心力衰竭(HF)(图4)[13]。

图4. CKD相关心肌病的发病机制
参考文献
[1]中国血液净化. 2024年8月, 第23卷, 第8期: 561-580.
[2]N Engl J Med 2022;386:2120-8.
[3]Journal of Human Hypertension (2023) 37:1–19.
[4]J Am Soc Nephrol. 2012 Sep 28; 23(10): 1725–1734.
[5]European Journal of Heart Failure (2018)20, 560–568.
[6]Nephrol Dial Transplant (1990) 5: 39-44.
[7]Kidney International, Vol. 67 (2005), pp. 333–340.
[8]Heart 2013;99:932–937.
[9]Hemodial Int. 2008;12:322–7.
[10]Journal of the American Society of Nephrology?28(8):p 2491-2497.
[11]Nephrol Dial Transplant (2000) 15 [Suppl 3]: 14–18.
[12]European Heart Journal (2017) 38, 1913-1923.
[13]Nat Rev Nephrol. 2019 Mar;15(3):159-175.
- 推荐文章
IgA肾病当前的诊断困境及生物标志物的研究进展
传统 vs. 新型盐皮质激素拮抗剂:谁在护心伤肾?——基于近3万例患者的肾脏安全性大揭秘
患者小课堂|你、我、他,谁更容易患肾脏病?一文速览
病例分享 | 20多岁冶金厂年轻小伙子咳嗽咯血,居然是这种罕见且凶险的肾病在捣乱!
氟氢可的松治疗成功纠正他克莫司诱导的低钠血症病例
世界睡眠日特别提醒!如何应对CKD患者的睡眠障碍
跟随国际IgA肾病联盟主席Jonathan Barratt教授,了解IgA肾病治疗最新进展——WCN 2025回顾
急性肾盂肾炎前瞻观察:哪些因素左右患者出院后的肾脏结局?
紧跟指南,护肾趁早!T2DM相关CKD治疗须与时俱进
肾域华章丨中大一院肾内科研究揭示IgA肾病伴肾病综合征患者的临床病理特征及与预后的关系
容易纠缠不清的病魔!泌尿系感染之肾盂肾炎,不容小觑
APRIL在IgA肾病治疗中的潜力
中国国医节 | 传承与创新:中西合璧挑战狼疮肾炎——黄芪的作用
蛋白尿与年轻人心搏骤停相关——CKD较严重者,风险更高
JASN|补体抑制剂治疗IgA肾病有望实现两个月给药一次?国际IgA肾病领军者Barratt教授最新研究揭晓
病例分享|不期而遇的困扰!丙肝患者短期内出现尿量减少,肌酐升高,警惕罕见的冷球蛋白血症肾病
2025年世界肾脏日:您的肾脏还好吗?早检查=保健康
ADPKD患者肾功能越差,疼痛频率越高,对睡眠的影响越显著
前沿进展|ORIGIN 2期研究结果重磅揭晓:阿塞西普长期治疗IgA肾病有效且安全
患者小课题|别让糖尿病伤了肾——如何早期发现糖尿病肾病
世界肾脏日丨早检查,保健康,拉紧心肾损伤警报线,优化T2DM相关CKD管理策略
Nature子刊|一文全解狼疮性肾炎相关CKD的管理理念与未来研究方向
狼疮性肾炎:突破传统,探索治疗新前沿
IgA肾病:IgA1免疫复合物的面面观
两款药物即将上市!FDA批准呋塞米注射液用于治疗CKD水肿;接受Obinutuzumab治疗狼疮肾炎的补充许可申请
慢性肾脏病患者的“症状关卡”,如何巧妙通关?
“心”感染,“肾”也跟着坏掉?感染性心内膜炎相关性肾炎,究竟是怎么一回事儿?
CKD相关心肌病的早期诊断与规范治疗
睡眠质量差,血液透析患者的“隐形杀手”!
WCN中国之声 | 郝传明教授:低氧诱导因子脯氨酰羟化酶抑制剂在慢性肾脏病贫血治疗中的两面性
探索替尔泊肽在肾脏疾病中的双重激动作用:GLP-1激动剂与潜在GIP介导的获益
什么是CKD相关心肌病?
IgA肾病的新兴疗法与当前争议
警惕!应用噻嗪类利尿剂后出现早期低钠血症,死亡风险或将大幅攀升!
高强度间歇训练显著降低老年人肾功能快速下降风险
指南共识 | 2024 ACR狼疮肾炎诊疗指南更新解读:从序贯治疗到联合免疫靶向的范式转变
病例分享丨中年男子3个月内肾功能快速恶化,原因究竟为何般?这种临床危重症,值得警惕
前沿进展丨常染色体显性多囊肾病患者的肾脏非线性生长模式与不良预后密切相关
糖衣炮弹下的肾脏危机!糖尿病最常见、最严重的并发症之一——糖尿病肾脏疾病
患者小课堂| IgA 肾病:症状背后的真相与应对策略
NEJM丨伊普可泮治疗IgA肾病Ⅲ期临床研究APPLAUSE-IgAN结果揭晓
狼疮性肾炎:流行病学特征与发病机制的最新研究进展
Kidney360|从成像模式看中国ADPKD患者临床特征及肾脏结局走向
NDT丨蛋白尿还是白蛋白尿?IgA肾病风险预测的关键指标再评估
WCN 2025|非奈利酮早期起始,持续治疗对于最大化患者临床效益至关重要
对激素(全身或肠道释放型布地奈德)耐药的肾病综合征范围蛋白尿的IgA肾病:他克莫司能否作为替代药物?
WCN 2025|非奈利酮显著降低蛋白尿,且疗效与安全性不受肾切除术史影响
病例分享 | 血透老人多病共存,内环境如同“纸糊“!棘手局面,肾病科医师如何破局?
WCN 2025|非奈利酮在肾移植后患者中安全有效,值得进一步探索
患者小课堂丨肾虚、肾亏是慢性肾炎吗?
NEJM前沿速递|阿曲生坦治疗IgA肾病Ⅲ期ALIGN试验的中期分析结果正式见刊
微小病变肾病,肾病综合征的第三大原因!“微小”病变也不容忽视,及时准确诊疗很关键
奥妥珠单抗有效保护LN患者的肾功能,显著减少LN发作,还具有减少糖皮质激素使用的潜力:NOBILITY试验事后分析
CKJ|浆细胞与补体或许是MN的潜在治疗靶点
揭秘BAFF、APRIL在IgA肾病中的作用以及治疗研究进展
